
骨細胞における自然免疫系MYD88シグナルは、細菌感染における骨溶解を直接制御する。
| 著者: | Tetsuya Yoshimoto, Mizuho Kittaka, Andrew Anh Phuong Doan, Rina Urata, Matthew Prideaux, Roxana E Rojas, Clifford V Harding, W Henry Boom, Lynda F Bonewald, Edward M Greenfield, Yasuyoshi Ueki |
|---|---|
| 雑誌: | Nat Commun. 2022 Nov 4;13(1):6648. doi: 10.1038/s41467-022-34352-z. |
- 骨細胞
- 細菌性骨感染
- MYD88

2022年米国骨代謝学会にて
筆者は真ん中、左が橘高瑞穂 先生、右が植木靖好 先生
論文サマリー
宿主−細菌叢間の相互作用は、自然免疫系の活性化において基本的な役割を果たしており、その主体は好中球やマクロファージ等の自然免疫細胞が担う。この相互作用の制御異常が、免疫介在性疾患に広く関与する一方で、骨構成細胞と細菌との相互作用が、骨格や免疫細胞の活性化に及ぼす影響については十分に理解されていない。
骨細胞は、骨基質に埋め込まれた最も豊富な骨構成細胞である。これまでに、骨細胞が細菌またその病原因子と直接相互作用する可能性が、in vitro実験から示唆されてきた。しかし、細菌病原因子が生体内で骨細胞を直接刺激するかどうか、また、刺激するとすれば、骨細胞上のどの自然免疫受容体が細菌病原体関連分子パターン(PAMPs)に反応するために使用されるかは不明であった。さらに、骨細胞は外部からの刺激に応答して様々なサイトカインを産生することが報告されているが、骨細胞由来の炎症性メディエーターが骨の恒常性や免疫細胞の制御に与える影響については解明されていなかった。
本論文では、まず骨細胞が、自然免疫受容体であるToll-like receptor (TLR)またその下流にあるアダプター分子MYD88を発現することを見出した。そこで、骨細胞T L R/MYD88経路が、細菌感染時における骨溶解や炎症等の生体反応にどのように寄与するか検討を行った。
その結果、1) MYD88が骨細胞選択的に欠失されたマウスでは、PAMPs誘導性の骨破壊から完全に保護されること (図1)、2)逆に、骨細胞における選択的なMYD88の発現のみで、PAMPs誘導性骨溶解モデルにおける骨溶解と炎症を引き起こすことができること (図2)、3) さらに、 in vitro実験から、TLR2およびTLR4アゴニストで刺激された骨細胞は、その前駆細胞である骨芽細胞よりも大きくRANKL (破骨細胞形成に必須のサイトカイン)を発現する能力を有すること、4) MYD88 経路を介したRANKLの発現には、転写因子であるCREB と STAT3 の活性化と安定性が重要であり、そして、これらCREB と STAT3の安定性向上には、それぞれ E3 ユビキチンリガーゼ FBXL19 と PDLIM2 が関与するという新規分子機構を見出した。4) また、MYD88阻害剤の投与により、歯周病モデルマウスの歯槽骨量減少が抑制されることを明らかにした。
これらの知見は、骨細胞がこれまでに知られていなかった骨における重要な細菌センサーであり、骨感染において自然免疫系MYD88シグナルをRANKL制御機構に統合することで骨溶解を直接制御していることを明らかにした。このように、本研究は骨格系における骨細胞MYD88経路の機能を明らかにし、骨細胞におけるMYD88および下流のRANKL制御分子を標的とした、感染性骨溶解の新しい治療法を開発するための遺伝的基盤を提供するものである。
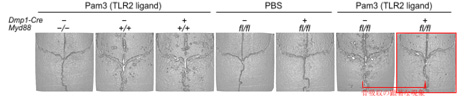
(図 1) MYD88が骨細胞選択的に欠失されたマウスでは、PAMPs誘導性の骨破壊から保護される。
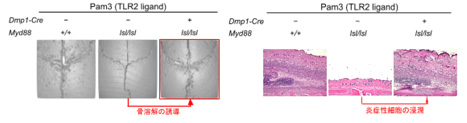
(図 2) 骨細胞における選択的なMYD88の発現のみで、PAMPs誘導性骨溶解モデルにおける骨溶解と炎症を引き起こすことができる。
著者コメント
広島大学歯周病態学講座の栗原英視先生の研究室での大学院時代は、歯肉上皮細胞を標的とした歯周炎予防がテーマでした。2016年から米国に留学することになり、当時ミズーリ・カンザス大学の植木靖好先生(現在はインディアナ大学)に師事しました。そこで、大学院時代とは全く異なる骨研究、特に本論文の主役である骨細胞研究にチャレンジし、上記研究結果を得ることが出来ました。留学のきっかけを与えてくださった日本学術振興会様、また本研究を遂行するにあたり、素晴らしい研究環境とご指導を下さいました植木靖好先生、そして多大なご助力を賜りましたLynda Bonewald先生、橘高瑞穂先生をはじめとした共著の先生方、滞米中いつも励ましてくれた日本人研究者の先生方にこの場をお借りして心から感謝申し上げます。(インディアナ大学・吉本 哲也)






