
自己免疫性関節炎におけるFoxp3+T 細胞からTh17細胞への分化転換の病理学的意義
| 著者: | Noriko Komatsu, Kazuo Okamoto, Shinichiro Sawa, Tomoki Nakashima, Masatsugu Oh-hora, Tatsuhiko Kodama, Sakae Tanaka, Jeffrey A Bluestone & Hiroshi Takayanagi |
|---|---|
| 雑誌: | Nat Med AOP |
- 制御性T細胞
- Th17細胞
- 滑膜線維芽細胞

論文サマリー
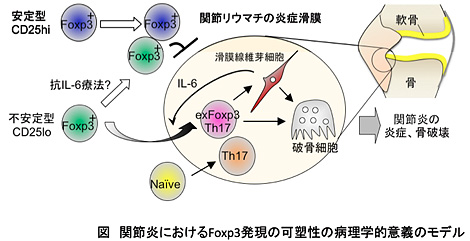
関節リウマチ(RA)は、関節の炎症と骨破壊を主な症状とする自己免疫疾患の一つである。Th17細胞はさまざまな自己免疫疾患の要因となりうるが、疾患形成過程における分化機構は不明な点が多い。一方で、制御性T細胞は、自己成分を認識するT細胞が、転写因子Foxp3を発現することで抑制機能を発揮し自己免疫疾患を抑制する。Foxp3の発現消失は自己免疫疾患発症の引き金となりうることからも、炎症状況下におけるFoxp3の安定性は議論の的となっているが、Foxp3+T細胞の分化可塑性の病理学的意義は不明な点が多い。そこで筆者らは、コラーゲン誘導性関節炎マウスを用いてこの課題に取り組んだ。まず細胞移入実験により、関節炎環境下でCD25の発現が低いFoxp3+T細胞がFoxp3の発現を消失してTh17細胞へ分化することを見出し、この細胞をexFoxp3Th17細胞と名付けた。次に、細胞系譜解析によりexFoxp3Th17細胞が炎症滑膜に多く集積することが分かった。さらに、試験管内の共培養により滑膜線維芽細胞がIL-6を産生することでexFoxp3Th17細胞への分化転換を促進することが明らかとなった。興味深いことに、exFoxp3Th17細胞は、滑膜線維芽細胞存在下においてナイーブCD4+T細胞由来のTh17細胞よりも強力に破骨細胞を誘導する ‘最強’の破骨細胞誘導性T細胞であることが分かった。またマイクロアレイ解析の結果、exFoxp3Th17細胞はSox4、CCR6、CCL20、IL-23R、RANKLを高発現し、これまで報告のない遺伝子発現パターンをもつTh17細胞サブセットであることが明らかとなった。生体レベルでの重要性を検証するため、コラーゲンを認識する細胞を多く含むCD25loFoxp3+T細胞をマウスに移入した上で関節炎を誘導すると、Foxp3発現の消失に伴い、関節の炎症と破骨細胞分化の亢進や骨破壊の増悪化を引き起こした。この結果からexFoxp3T細胞の生体レベルでの関節炎誘導能が明らかとなった。重要なことに、疾患活動性の高いRA患者の炎症滑膜では、分化転換の過渡期と考えられるFoxp3とIL-17の両方を発現するT細胞が多く存在することから、RAにおいても分化可塑性をもつFoxp3+T細胞が病因に関与することが示唆された。本研究により、関節の炎症と骨破壊を増悪化する新しい病原性Th17細胞(exFoxp3Th17細胞)が同定され、滑膜線維芽細胞の産生するIL-6によりFoxp3+T細胞から分化転換することが分かった。抗IL-6療法がTreg/Th17バランスを改善することを鑑みると、分化可塑性をもつFoxp3+T細胞がRAの増悪化の鍵を担っている可能性が示唆される。Foxp3+T細胞の分化可塑性がTCRのレパトアと関連性をもつかどうか、今後の解析が待たれる。exFoxp3Th17細胞は、RAをはじめとするさまざまな自己免疫疾患の治療標的となる可能性を持つ。exFoxp3Th17細胞の病原性を司る分子基盤の解明により、自己免疫疾患の新しい治療薬や診断マーカーの確立への道を拓くことが期待される。
著者コメント
RAの病態形成においては‘関節特異的’な滑膜線維芽細胞の重要性が知られていますが、その病原性のメカニズムは未だ不明な点が多いです。本研究では、滑膜線維芽細胞によって分化し、関節炎の炎症と骨破壊を増悪化させるT細胞の亜集団を同定できました。一方で、関節炎の増悪化にはT細胞による滑膜線維芽細胞の活性化も必要です。このように、自己免疫疾患の病態形成における間葉系細胞と免疫細胞の相互作用の病理学的意義の解明を通して、疾患治療法の基盤の確立に貢献できればと存じます。本研究の遂行にあたり多大なご協力を賜りました、高柳先生をはじめとする共著の先生方および研究室員の皆様に厚く御礼申し上げます。(東京大学大学院医学部研究科 免疫学・小松 紀子)






