
Folliculinによる代謝制御を介した破骨細胞分化の新たな制御機構
| 著者: | Baba M, Endoh M, Ma W, Toyama H, Hirayama A, Nishikawa K, Takubo K, Hano H, Hasumi H, Umemoto T, Hashimoto M, Irie N, Esumi C, Kataoka M, Nakagata N, Soga T, Yao M, Kamba T, Minami T, Ishii M, Suda T |
|---|---|
| 雑誌: | Journal of Bone and Mineral Research, 2018 Oct;33(10):1785-1798. |
- 破骨細胞
- 代謝
- プリン作動性シグナル

論文サマリー
破骨前駆細胞が破骨細胞に分化する際には、細胞の代謝状態と共に遺伝子発現が劇的に変化する。近年、破骨前駆細胞の分化過程における代謝状態の変化と遺伝子発現変化の密接な関係とその重要性が明らかにされつつある。重要な例としては、ミトコンドリア生合成のマスター転写因子Pgc1βが破骨細胞分化に必須であることや、破骨細胞分化過程において代謝状態の酸化的リン酸化へのシフトがエピゲノム制御を介して破骨細胞分化に寄与している事などが挙げられる。また、破骨細胞の分化においてはプリン作動性シグナルの重要性が数多く報告されており、プリン代謝の制御が破骨細胞分化に重要な役割を果たす事が示唆される。その一方で、これら細胞代謝制御の上流因子に関しては未解明のままであった。
本研究では、Folliculin(FLCN)分子が細胞の分化と代謝制御において極めて重要な役割を果たすという我々のこれまでの研究成果に基づき、代謝制御を介した破骨細胞分化の新たな制御機構の解明に取り組んだ。
FlcnコンディショナルノックアウトマウスをMx1-Creトランスジェニックマウスと交配し、pIpC投与により生後11週のマウス破骨前駆細胞でFlcn遺伝子の欠損を誘導すると、破骨細胞の増加と骨吸収の増加により、マウスはわずか3週間で極めて重篤な骨粗鬆症を発症した(図1)。
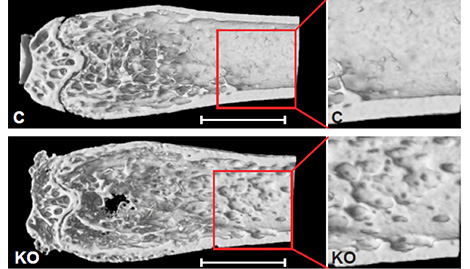
図1 pIpC投与後3週目におけるマウス大腿骨のμCT像 Flcn f/f;Mx1-Cre- (C: Flcn WT) mice (upper panel), Flcn f/f;Mx1-Cre+(KO: Flcn KO) mice (lower panel)
Flcn欠損破骨前駆細胞はRANKLへの感受性が大きく亢進し、細胞自律的に破骨細胞への分化が亢進していた。網羅的遺伝子発現解析では、Flcn欠損破骨前駆細胞では酸化的リン酸化経路とプリン代謝経路に関与する遺伝子の発現が優位に亢進していた。また、Flcn欠損破骨前駆細胞ではMITFファミリーの転写因子であるTfe3が核内に移行し、その転写標的遺伝子の発現が亢進していた。更に、酸化的リン酸化経路/ミトコンドリア生合成のマスター転写因子であるPgc1αとPgc1βは、そのプロモーターにTfe3が結合し、直接の転写標的遺伝子として発現が誘導される事が、ChIP-qPCRとqRT-PCRで明らかになった。
これらの結果をサポートする様に、メタボローム解析はFlcn欠損細胞における酸化的リン酸化の亢進とプリン代謝物の増加を示した。中でもATPとアデノシンのFlcn欠損細胞における増加は目を見張るものが有り、プリン代謝物のオートクライン・パラクラインからなるプリン作動性シグナルの亢進が、Flcn欠損破骨前駆細胞の分化亢進に寄与している可能性が考えられた。実際にFlcn欠損細胞の培養上清は、Flcnが正常な破骨前駆細胞においても破骨細胞分化の指標となる遺伝子の発現を亢進させた。「制御されたATPの細胞外へのリリース」「細胞表面でのADP-AMP-アデノシンへの代謝」「プリン作動性受容体の刺激」で構成されるプリン作動性シグナルループを阻害する事で、Flcn欠損破骨前駆細胞の破骨細胞への分化亢進は抑制された。以上の結果より、Flcn-Tfe3-Pgc1軸は酸化的リン酸化とプリン代謝を含む細胞内代謝の再構成を介して破骨細胞の分化を制御していることが明らかになった(図2)。
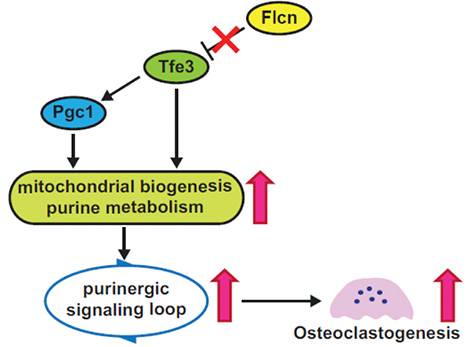
図2 Flcn-Tfe3-Pgc1軸による代謝制御を介した破骨細胞分化の新たな制御機構
本研究で破骨細胞の分化に重要な役割を果たすことが明らかになったFLCN遺伝子は、遺伝性腎細胞癌症候群の原因となるがん抑制遺伝子として2002年に新たに単離されたものです。私共はこれまでにFLCNが代謝制御を介して細胞の分化・増殖に重要な役割を果たしていることを見出して来ました。上述の様に破骨前駆細胞が分化する過程では代謝状態の変化が必須な事から、破骨前駆細胞におけるFlcnの重要な役割が予想されました。しかし、Flcnノックアウトマウスがこれ程迄に重篤な骨粗粗鬆症を示すとは思いもしませんでした。専門外の破骨細胞の研究に当初は戸惑いましたが、須田先生、石井先生、西川先生、田久保先生はじめ多くの先生方からお力を頂き、本研究を世に出すことが出来ました。この場をお借りして御礼申し上げます。(熊本大学国際先端医学研究機構/がん代謝学講座・馬場 理也)






