
人が通らない道を通りたかった。一人が通れば、道はどんどん広くなる。
- ぺリオスチン
- OB-カドヘリン
- メダカ

メダカの水槽の前で記念撮影しました。
私の骨研究についてまとめると次の4つになります。
(1) 破骨細胞分化系を確立し、TNFαが破骨分化因子であることを明らかにした。
(2) OB-カドヘリン/カドヘリン-11を発見し、OB-カドヘリンは頭蓋骨形成に寄与する。
(3) 歯根膜・骨外膜に発現しているマトリックス蛋白質を、ぺリオスチンと命名した。ぺリオスチンは歯と骨のリモデリングに機能し、特にコラーゲン架橋を促進する。
(4) メダカの骨形成のシステムを確立し、多くの変異体から原因遺伝子を明らかにするとともに、造骨と破骨細胞を可視化したトランスジェニックラインを宇宙ステーションで飼育し、無重下での骨量減少を見い出している。
これから私の研究の物語を始めますが、研究開始から時代順にこれまでどのようにして研究してきたか、できるだけありのままを述べることにします。
骨研究を始める前に
まず初めに骨の話を始める前に、医学や歯学を学んでいないのに、骨研究を始めた理由について述べようと思います。東工大で高分子化学を学んだ後に、帝人の中央研究所に入り、当初は人工血管を研究していました。当時は石油ショックの大不況で、帝人も何か新しいことを始める必要があるということで、遺伝子工学の研究室ができました。この研究室の一番最初の研究員だった私が考えたのが、帝人が手掛けていた抗体製剤を遺伝子工学で作ろうというものでした。東大で遺伝子工学をほんの少し勉強した後に、佐賀医科大学でモノクロナル抗体を研究していた渡邊先生と一緒に研究することになりました。その最初の論文がヒトとマウスとのキメラ抗体でした。今大流行のヒト型抗体製剤です。当時、穂積先生がNatureに出した論文には負けましたが、日本では最初の論文でした(Nishimura et al. Can. Res. 1987)。その後帝人を退社し、九大に移った渡邊先生の研究室の助手になり、すぐにバーゼル免疫学研究所の研究員になりました。キメラ抗体のような応用研究ではなく、自分で免疫の秘密を解き明かす研究がしたくなったのです。渡邊先生がバーゼル研の出身で、所長のメルシャース先生とコネがあったのです。バーゼル研は世界最高の研究所の一つであり、有名な研究者と若手の優秀な研究者が切磋琢磨しているところでした。前所長のヤーネ博士がイディオタイプネットワークで、研究員であるケーラー博士がモノクロナル抗体でノーベル賞をすでにもらっており、利根川さんがノーベル賞をもらう直前でした。テーマは自由でした。今まで全くフリーにテーマを考えたことがなく、何をしていいのか困りました。1か月後には所長のインタビューがあり、テーマの説明をしなければなりません。結局、所長に英語がへたすぎてディスカションできないからと言われて英語の家庭教師をつけてもらい、その程度の英語力ですから日本人を頼るしかなく、日本への帰国が決まっていた阪口先生のとった遺伝子lambda 5の続きをやることにしました。lambda 5はプレB細胞特異的に発現しており、その発現の制御機構だったら、これまでの研究にも近くて何とかやれそうだったのです。このlambda 5の転写調節を調べているときに偶然見つかったのがVpreB遺伝子です(Kudo A, et al., EMBO J. 1986, 被引用数CI=304)。VpreB とlambda 5が会合してsurrogate L 鎖になり、さらにH 鎖と会合してプレB細胞レセプターになります。1989年の国際免疫学会のシンポジュウムでこの成果を発表できたのは非常に名誉なことでした。一方、このプレB細胞レセプターの機能を証明するのが難しく、渡邊先生のところで一緒だった北村さんがドイツのラジェイフスキー教授のところでノックアウトマウスの作成を始めていたので、共同研究を申込みにドイツに行きました。1980年代の終わりですから、ノックアウトマウスをできるところが少なくヨーロッパではラジェイフスキー教授ぐらいでした。ノックアウトマウスの解析から、プレB細胞レセプターはB細胞分化においてH鎖をチェックして、成熟B細胞へ分化を進める働きを持っていることが証明されました(Kitamura et al, Cell 1992, CI=561、この論文は2010年国際免疫学会誌の、免疫学の土台を造った論文に選ばれてます)。この成果により、プレB細胞レセプターは細胞生物学の教科書にも免疫学辞典にも載っています。この間、一度九大に戻って助教授になったものの、再度バーゼル研でこの仕事をしましたので、スイス滞在は5年におよび40歳になってました。1992年、子供の教育のこともあり日本で職探しをして見つかったのが、ドイツ発祥の国際企業であるヘキスト社の日本研究所でした。
骨の研究開始
この研究所は、会社に関わらず当時先端的な分子生物学研究を志向しており、新規遺伝子のクローニングを行ってました。そのチームリーダーとして迎えられ、そこでOBカドヘリン/カドヘリン-11、ぺリオスチンに出会ったのです。1994年12月、縁あって東工大の教授として迎えていただいたとき、この2つの遺伝子を東工大に譲っていただきました。東工大ではどんな研究でもできたのですが、やはりプレB細胞レセプターの続きの免疫研究と、骨の研究の2本立てで行くことにしました。その当時、骨の研究は骨芽細胞も破骨細胞もまだ黎明期で、マスター遺伝子も見つかっていませんでした。B細胞分化が特異的な遺伝子のクローニングから発展したこともあり、骨の重要な遺伝子のクローニングとその機能解析に主眼をおいたのです。骨芽細胞はヘキストの遺伝子があったので、ノックアウトマウスを作って、その機能解析を行うこととし、破骨細胞は遺伝子クローニング用の細胞分化系を作ることから始めました。そのとき、今長寿研にいる竹下さんがヘキストを辞めていましたので、東工大に来ていただいて破骨細胞分化系を作ってもらいました。この研究は2000年のJBMRに掲載され(Takeshita et al, J. Bone Miner. Res, 2000, CI=274)、同時期にこの系を用いてTNFαが破骨細胞分化因子であることを発表しました(Azuma et al, J. Biol. Chem. 2000, CI=450)。一方、当初の目的であったRANKL, RANK, DC-STAMPのクローニングはできませんでしたが、特にTRAFとの関連で破骨細胞分化制御について続けてJBMRに発表しました(Kaji et al, J. Bone Miner. Res. 2001, Kanazwa et al, J Bone Miner. Res. 2003, 2005a, 2005b) 。骨芽細胞の方は、OB-カドヘリンに関してはすでにヘキスト社で論文にしておりましたが(Okazaki at al. J. Biol. Chem. 1994, CI=202)、ぺリオスチンについては、骨外膜と歯根膜の特異的発現からぺリオスチンと命名した最初の論文を1999年に発表しました(Horiuchi et al, J. Bone Miner. Res. 1999, CI=478)。今から振り返ると1999-200年というのは被引用数の高い重要な論文が相次いで発表できた年でした。優秀な共同研究者が一緒に仕事をしてくれた御蔭です。ついでにこの年、最初に作ったノックアウトマウスの解析からCD9が精子と卵子の融合に必須の因子であることが見つかりました(Kaji et al, Nat. Genet. 2000 CI=325)。CD9は破骨と造骨を両方制御するカップリング因子のようなものと考えてましたので、少し残念でした。OB-カドヘリンに関しては、その後カドヘリン-11とも呼んでますが、特に頭蓋骨形成を始めとする骨形成制御因子としてJBMRに連報で発表しました(Kawaguchi et al. J Bone Miner. Res. 1999, 2001a, 2001b, Kii et al. J. Bone Miner. Res 2004)。私の論文がJBMRに多いとよく言われますが、私が骨研究の新参者でしたので、同じジャーナルに出すことで名前を覚えてもらう必要があったのです。OB-カドヘリンに関しては骨癌との関係も深く最初の論文を当時東大の病理にいた鹿島さんと発表しました(Kashima et al. Am. J. Pathol. 1999)。現在は私はOB-カドヘリン研究をしていませんが、リューマチの重要な因子として注目されてます。
ぺリオスチン研究
東工大ではノックアウトマウスの作成ができなかったので、共同研究をお願いしてマウスを作成していたのですが、ぺリオスチンノックアウトはなかなかできませんでした。ようやく7年かけて3か所目で作っていただいたのは、遺伝研の相賀先生の研究室でした。ぺリオスチンは他の遺伝子のように既知ではなく、特に発現の特異性と蛋白質構造が面白かったので、自分の手で一分野を作れると思ってました。しかし、ようやくできたノックアウトマウスはほとんど異常がなくがっかりしましたが、現北大の網塚先生が歯根膜の異常と切歯の萌出不全を見つけてくれて、2005年のアメリカ骨代謝学会で口演で発表しました。引き続き骨の異常を探しているときに、アメリカから突然ぺリオスチンノックアウトマウスの論文が出て、非常にショックでした。まさかぺリオスチンノックアウトマウスを他で作っていると思いもしなかったのです。あわててBBRCに発表しましたが(Kii et al, Biochem. Biophys. Res. Com. 2006)、一挙に競争が始まったのです。この競争は心臓病に飛び火し、アメリカで2つ目のノックアウトマウスが作成されており、心筋梗塞と拡張性心筋症にぺリオスチンが関与していると報告されました。同時期に私達も心筋梗塞の心破裂をぺリオスチンはブロックするという画期的な結果を得て、JEMに発表しました(Shimazaki et al. J. Exp. Med. 2008, CI=196)。骨形成に関しては皮質骨のリモデリングに関与し、コラーゲン架橋を促進することを明らかにし、JBCに発表しました(Kii et al, J. Biol. Chem. 2010, Maruhashi et al, J. Biol. Chem. 2010)。そしてぺリオスチンの種々の機能を解説する総説を発表しました(Kudo A. Cell. Mol. Life Sci. 2011, Conway et al. Cell. Mol. Life Sci. 2014)。現在ぺリオスチン研究は、歯根膜、骨外膜の重要なマーカーに留まらず、癌、心臓病、創傷、アレルギー、脳梗塞に広がっており、近年飛躍的に論文が増えています。そしてアメリカ骨代謝学会の教科書、Primer on the Metabolic Bone Diseases and Disorders of Mineral Metabolismの第8版に、ぺリオスチンがマトリックス蛋白質の1つとして加わりました。
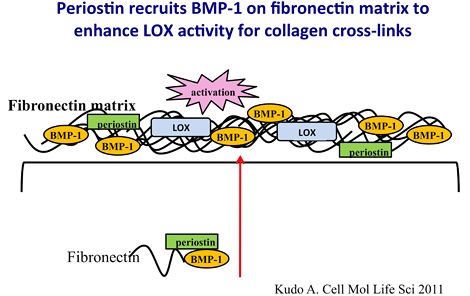
この図はCellular and Molecular Life Sciencesの2011年、68巻, 19号の表紙を飾りました。
ぺリオスチンがコラーゲンの架橋を促進することを現しています。
メダカ骨発生・骨形成研究
In-vivo研究の重要性を常に考えており、東工大でノックアウトマウスの作成ができなかったことも併せて、他の実験動物を導入することを考えていました。最初はゼブラフィッシュを扱い始めましたが、変異体のスクリーニングの機会を得ることができたときに、まだ手つかずであったメダカの変異体を作成することにしました。それと同時期にそれまでメダカの骨形成について知見がなかったため、一からメダカの骨形成を研究することにしました。スクリーニングでは骨異常変異体を取りたかったのですが、他の変異体でもその器官異常が興味深いものについては研究の対象としました。この変異体スクリーニングがきっかけでメダカゲノムのプロジェクトが始まり、その塩基配列がNatureに発表されました。その情報を使ってpositional cloningが可能になり、変異体の原因遺伝子を明らかにして、その多くをDevelopmental Biologyに発表しました。また新規の発見としては、底板に発現するWnt4bが椎骨のパターニングを制御するというものでした(Inohaya et al, Development 2010)。骨に関してはその多くは骨芽細胞に関与しており、骨発生に機能するものでした。そして破骨細胞についても解析することを始め、メダカ破骨細胞分化遺伝子のクローニングと、破骨特異的トランスジェニックメダカの作成により生きたまま破骨細胞が観察できる系を確立しました(Chatani et al, Dev. Biol. 2011)。破骨細胞が融合する様子もin-vivoで見れます。 またTilling法による変異体の作成、そして2013年からはTALEN法によるノックアウトメダカの作成も始まり、トランスジェニックとノックアウトを掛け合わせたメダカも作成され、骨発生をよりダイナミックに観察できるようになりました。一方、2000年に入ってからJAXAの宇宙ステーションきぼう棟における小型魚類水棲装置の開発が始まりました。無重力において骨量が減るのは解決しなければならない緊急の課題であり、まだマウスの飼育施設が宇宙ステーションにはないので、メダカが最適候補として浮かび上がってきました。途中、実験延期があったなか、2012年に水棲飼育装置がきぼう棟に完成し、2012年10月、最初の実験がosterix-DsRed/TRAP-GFPのダブルトランスジェニックメダカで始まりました。無事2か月の飼育に成功し、現在持って帰ってきたサンプルの解析中です。ついで2014年2月に短期の実験としてこのダブルトランスジェニックメダカの蛍光観察を宇宙ステーションで行いました。宇宙でもメダカの骨量減少が見られており、特に骨代謝が激しい咽頭歯を支える咽頭歯骨が顕著でした。
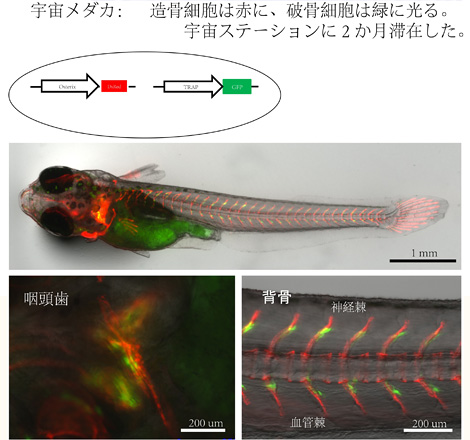
宇宙ステーションで長期飼育したダブルトランスジェニックメダカです。
生きたまま骨芽細胞と破骨細胞が観察できます。
研究人生
免疫から骨へ、細胞からマウス、メダカへ、一人の研究者としては多くのテーマを手掛けた人生でした。ただ運に任せて研究をしてきたような気がします。不思議なのは少なくとも免疫をやっていた30代は不遜にも、ここで歴史に残るような新しい発見ができたらいつ死んでもいいと思っていました。もちろん、名誉もお金もいらないと思ってました。そして50歳をこえたら研究は無理と思ってましたが、もう60歳をこえました。若い頃の元気はなくなってきましたが、まだ慕ってくれる学生がいるうちは研究を続けるつもりです。

カザフスタンのバイコヌール基地にあるソユーズ発射場の看板の前で。
東工大、JAXA, ロシアの関係者で記念撮影。
終わりに
骨形成の研究に東工大で最も欠けていた分野は組織学でした。マウスの解析では網塚先生、そしてメダカの解析では東京医科歯科大学の高野先生に長い間共同研究をお願いして、一緒に論文を出せたことが、幸せでした。そして多くの共同研究者に恵まれた結果、曲りなりにもこのトップランナーとして記事を書いている所以です。いままでの御厚意を感謝いたします。結局、私の時代はどんな遺伝子でもそれに決めて実験を続ければそれなりの研究ができた幸せな時代でした。被引用数はそこそこ高い論文を出せましたが、それでもNature, Cellは一報も出せませんでした。 東工大は技術もなく、お金もなく、あるのは優秀な学生でしたが、その学生の能力を十分に伸ばしてあげることができたのかどうか。彼らの能力を持ってすれば、もう少しましな研究室に居れば、Nature, Cellに論文を出せたのだろうと思うこともあります。最後に日本骨代謝学会はやさしい学会でした。門外漢の私を迎い入れ、いつもご教授していただいた皆様に感謝申し上げます。






