
骨芽細胞におけるFam20C過剰発現は、皮質骨の形成と破骨細胞性骨吸収を促進する
| 著者: | Katsutoshi Hirose, Takuya Ishimoto, Yu Usami, Sunao Sato, Kaori Oya, Takayoshi Nakano, Toshihisa Komori, Satoru Toyosawa |
|---|---|
| 雑誌: | Bone. 2020 May 13:115414. |
- FAM20C
- リン酸化
- 酸性リン蛋白質

論文サマリー
生体硬組織である骨や歯には、骨シアロ蛋白質、DMP1、DSPP等のSIBLINGsファミリーに属する酸性リン蛋白質が多く含まれている。これらの基質蛋白質は、翻訳後修飾過程で高度にリン酸化され、多数のリン酸基が付加されて負に荷電する。高度な負荷電体となった蛋白質は、Ca2+結合能を獲得して、骨の石灰化前線で石灰化制御に関与すると考えられている。しかし、生体硬組織におけるこれらの蛋白質のリン酸化の意義については未だ明らかにはなっていない。
Fam20C (family with sequence similarity 20 member C)は、核や細胞質に局在する既知のキナーゼとは異なり、近年発見された分泌蛋白質のリン酸化を担うキナーゼである。Fam20Cは、歯や骨で高発現することが報告され、我々は分泌過程にある骨基質蛋白質がゴルジ装置内でFam20Cによりリン酸化されることを以前に報告した(Histochem Cell Biol, 147:341-, 2017)。Fam20Cの機能は、ヒトのFam20C機能不全 (Raine症候群)やFam20C欠失マウスが骨軟化症様の骨変化を示すため、骨形成に重要であると考えられている。しかし、この疾患患者と欠失マウスはFGF23関連低リン血症を発症して、骨形成に全身性の低リン血症が影響するため、骨形成局所におけるFam20Cによるリン酸化の役割を検討することは困難である。
本研究は、I型コラーゲンプロモーターを用いて作製したFam20C過剰発現マウス (Fam20C-Tg)では、血清リン濃度に異常はみられなかったため、Fam20C過剰発現による骨変化から、Fam20Cによるリン酸化の役割を検討した。Fam20C-Tgは、野生型マウスと比較して、体格に変化はなかった。網羅的リン酸化解析等により、Fam20C-Tgの骨組織では、骨基質を含む様々な蛋白質のリン酸化亢進が確認された (図1)。Fam20C-Tgの骨変化として、皮質骨では、骨量、石灰化速度、骨形成速度が増加していた (図2 A-C)。また、皮質骨と海綿骨における破骨細胞性骨吸収が促進していた(図2 矢印B, D)。
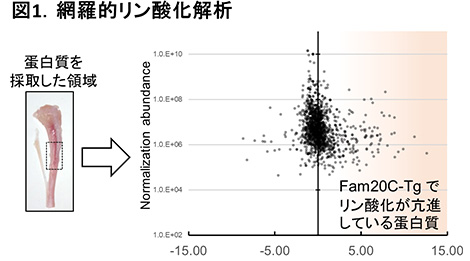
図1.網羅的リン酸化解析 (本論文より改変)。Fam20C-Tgの骨組織では、骨基質蛋白質を含む様々な種類の蛋白質のリン酸化が亢進している (橙色領域の黒点)。
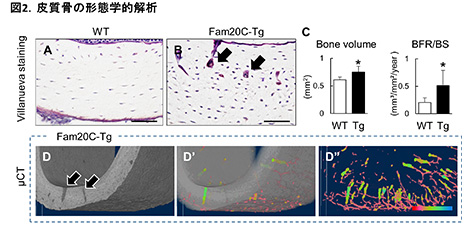
図2.皮質骨解析 (本論文より改変)。野生型 (WT)マウスと比較して、Fam20C-Tgマウスでは、骨量および石灰化速度に起因する骨形成速度の増加が認められた (A-C)。また、骨吸収亢進を示す多孔領域が有意に増加しており (矢印 B)、µCT解析により多孔領域は連続性のあるハバース管様の構造であることが明らかとなった (D-D”にかけて透過性が上昇)。
本研究は、生体の骨組織では、骨芽細胞/骨細胞の分泌蛋白質のリン酸化という翻訳後修飾が、石灰化を介した骨形成や、破骨細胞性骨吸収に重要であることを示したものである。
著者コメント
骨を構成する蛋白質のリン酸化の意義という、骨研究の新しい分野へのチャレンジでした。生体硬組織でのリン酸化解析の前例は乏しく、Fam20C-Tgの骨のリン酸化状態の解析には特に苦労しました。多角的にリン酸化の役割を解析し、その結果を今回論文として形に残すことができて大変嬉しく思っています。研究を進めれば進めるほど、骨に対する謎と興味は深まるばかりです。貴重なお時間を惜しみなく費やしてくださった責任著者の豊澤教授にはとても感謝しております。また、ご指導頂きました長崎大学の小守壽文先生、大阪大学の中野貴由先生、石本卓也先生、口腔病理学教室の先生方に厚く御礼申し上げます。(大阪大学大学院歯学研究科 口腔病理学教室・廣瀬 勝俊)






