
TNFRSF11Aに関連する異骨性骨硬化症:2例目の報告と表現型スペクトルの特徴付け
| 著者: | Xue JY, Wang Z, Shinagawa S, Ohashi H, Otomo N, Elcioglu NH, Nakashima T, Nishimura G, Ikegawa S, Guo L. |
|---|---|
| 雑誌: | J Bone Miner Res. 2019 Oct;34(10):1873-1879. |
- RANK
- 異骨硬化症
- 大理石骨病

論文サマリー
骨硬化症は全身的な骨濃度の上昇をきたす疾患の総称である。代表的な疾患に大理石骨病(osteopetrosis)や異骨性骨硬化症(dysosteosclerosis)がある。TNFRSF11A(別名RANK)は、常染色体劣性遺伝7型大理石骨病(osteopetrosis, autosomal recessive 7; OPTB7)の原因遺伝子として知られていた。しかし最近、我々の研究チームは、RANK変異による異骨性骨硬化症の1例を世界で初めて報告した(Guo et al. J Hum Genet 2018)。本研究では、2例目のRANK変異による異骨性骨硬化症を報告し、OPTB7症例と2例のRANK変異による異骨性骨硬化症とを比較し、RANK変異による骨硬化症の表現型スペクトルを明らかにした。
異骨性骨硬化症は、骨濃度の上昇、脊椎の形成障害、長管骨と短管骨の骨幹端部の拡大などの特徴を持つ骨硬化症である。遺伝的な異質性が知られており、いくつかの原因遺伝子があると推定される。先にSLC29A3が原因遺伝子として発見されていた。最近、我々の研究チームは新しい二つの原因遺伝子(RANKとCSF1R)を同定した。しかし、それらの表現型スペクトルの特徴はまだはっきりしていない。
新たに発見した日本人の異骨性骨硬化症患者の原因遺伝子を同定するために、上記の3つの既知の原因遺伝子を探索した。その結果、RANKのホモ接合変異を発見した。この変異c.1441C>Tは、単純なコドンの解釈からはナンセンス変異p.Gln481*である。しかし、塩基置換はエクソンとイントロンの境界で起きているので、スプライシング異常の可能性もあると考えた。患者由来のRNAを用い、RT-PCRで調べると、確かにスプライシング異常があることがわかった(図1)。公共データベースには、RANKのトランスクリプトが五つ載っている。このスプライシング異常は、その中の二つにしか影響しない。トランスクリプトにより変異の効果が違うという現象は、1例目の患者でも発見された。更に、体外分化誘導実験の結果から、患者の単球の破骨細胞への分化能力が低いことが分かった(図2)。
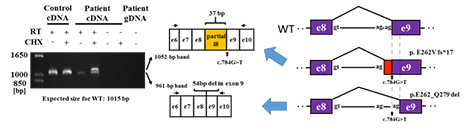
図1 変異によるRANKのスプライシング異常
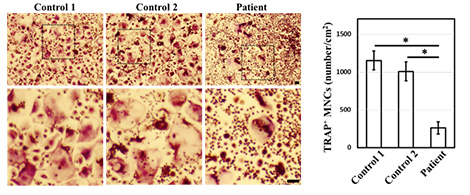
図2 患者由来の単球から破骨細胞への分化異常
RANKは単球/マクロファージ系列の細胞から破骨細胞への分化を誘導するキーファクターとしてよく知られている。RANKの五つのトランスクリプトには、どのような機能があるのかは、まだはっきりしていない。2例の異骨性骨硬化症の変異は共に、スプライシング異常を起すのに対し、OPTB7のRANK変異はスプライシングとは無関係で、全てのトランスクリプトの消失を引き起こす。異骨性骨硬化症とOPTB7の表現型の違いは、このような遺伝子機能に対する変異の効果の違いに起因すると考えられる。
著者コメント
私は中国の首都医科大学の修士課程在学中から、遺伝子の変異に興味を持っていました。2018年より、横浜市立大学の博士課程に進学し、理化学研究所生命医科学研究センター・骨関節疾患チーム(池川志郎チームリーダー)で、骨関節の単一遺伝子病の研究を始めました。
本研究は私の日本での最初の仕事でした。論文の査読者のコメントによって、患者さんの破骨細胞のインビトロアッセイが必要になりました。細胞株を用いた実験の経験はありましたが、患者さんの貴重な血液を頂いて実験したことは、一度もありませんでした。分化実験をするチャンスは1度しかないので、自分の血液を使って破骨細胞の分化誘導条件を検討して、最適な条件を見つけました。
レヴューは厳しかったですが、研究室や共同研究者(品川知司先生(群馬大)、中島友紀先生(東京医科歯科大)他)の皆様のおかげで、乗り越えることができました。心より感謝申し上げます。(理化学研究所・薛 婧怡)






