
ゼブラフィッシュ鱗において、表皮が骨芽細胞の発生を介して、骨の形態形成を制御する
| 著者: | Iwasaki M, Kuroda J, Kawakami K3 Wada H. |
|---|---|
| 雑誌: | Developmental Biology, 2018 May 15;437(2):105-119. |
- ゼブラフィッシュ
- 鱗
- shhシグナル

論文サマリー
多様な骨の形態は、骨芽細胞が特定の場所に局在することにより作り出されている。本研究で、我々は、皮骨であるゼブラフィッシュの鱗が、どのような分子メカニズムによって形作られるのかを調べた。
まず初めに、GFPトランスジェニック系統を用いて、鱗が形態の異なる2種類の骨芽細胞で構成されていることを示した(図A)。鱗の裏面にある1層の扁平な細胞(i)と、鱗の辺縁(成長端)にある細長い細胞(ii)である。このうち扁平な骨芽細胞(i)は、細胞接着面が仮足を激しく伸ばし、鱗の成長に伴い面積が増大していた(図B)。このとき骨芽細胞の増殖は生じておらず、従って骨芽細胞の数は増加しなかった。このことから、鱗の成長は、骨芽細胞自体の成長を伴い生じることが示された。
これまでゼブラフィッシュの鰓蓋骨や鰭条骨の形成の際に、Hedgehog signaling pathwayが骨芽細胞の増殖や局在に働くことが示されている。鱗では成長端にある細長い細胞(ii)を覆う表皮細胞でsonic hedgehogが発現していた。薬剤処理によってHhシグナルを阻害すると、成長端にある骨芽細胞(ii)のみが形成されず、鱗の成長も阻害された。つまり、鱗形成において、表皮から分泌されるShhが、特定の骨芽細胞の分化に働き、この骨芽細胞が骨の成長を引き起こしていることが示された。
表皮におけるshhの発現領域は、鱗を縁取る領域に、一定方向・一定間隔で並んでいる。一方、表皮の平面極性(Planar cell polarity)は、Wnt/PCPシグナルにより制御されていることが知られている。そこで、Wnt/PCPシグナルの受容体であるFzd3aの細胞内ドメインを除去した変異タンパク質(dnFzd3a)を表皮特異的に発現させ、Wnt/PCPシグナルを阻害した。その結果、shhの発現領域が一定方向に並ばず、ランダムな方向へ傾く異常を示した。それに伴い、鱗の成長方向も異常を示し、渦を巻く個体も見られた(図C)。本研究によって、表皮におけるWnt/PCPシグナルがshhの発現パターンを制御し、さらにShhが特定の骨芽細胞を分化させることによって、骨を一定方向へ伸長させることが明らかとなった。
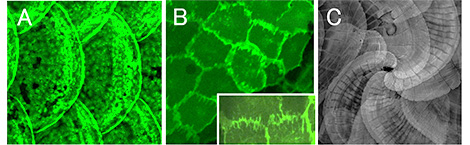
A: 骨芽細胞をGFPで標識するgSAIzGFFM848Aトランスジェニック系統
B: 骨芽細胞の細胞接着面が仮足を伸ばす様子
C: 表皮のWnt/PCPシグナルの阻害により引き起こされた、鱗の異常パターン
著者コメント
魚の鱗を用いた組織学的な研究の歴史は古く、私たちが観察した骨芽細胞もすでに記載されていますが、その役割は分かっていませんでした。GFPトランスジェニック系統を用いin vivoで細胞動態を観察し、骨芽細胞が激しく仮足を伸ばしながら、大きくなることがわかったときは、本当に驚きました。それと同時に、何十年も前に同じ細胞を詳細に観察した人々がいたことに感慨深い思いがしました。鱗には、骨芽細胞の他に破骨細胞も存在します。私たちの研究から、側線鱗と呼ばれる特殊な形態の鱗は、骨リモデリングによって形づくられることが分かっています(Wada et al., 2014)。今後も、これらの細胞の動態を調べることによって、生物の形づくりの謎に迫っていきたいと思います。最後に、本研究を行うにあたり協力をして頂いた全ての方々に感謝致します。(北里大学 一般教育部 生物・岩崎 美樹)






