
骨破壊性T細胞による生体防御機構
| 著者: | Tsukasaki M, Komatsu N, Nagashima K, Nitta T, Pluemsakunthai W, Shukunami C, Iwakura Y, Nakashima T, Okamoto K, Takayanagi H. |
|---|---|
| 雑誌: | Nature Communications, 2018 Feb 16;9(1):701. |
- 口腔細菌
- T細胞
- 破骨細胞

著者(左)と高柳広教授。学会で訪れたウィーンのレストランにて
論文サマリー
脊椎動物の最外層を構成する皮膚と粘膜は、タイト結合によって強固に連結された上皮細胞シートにより覆われており、自己と非自己との境界を規定し病原体の侵入を物理的に拒んでいる。消化管の入り口である口腔は、胃酸や消化酵素による選択を受けた細菌のみが生着する腸管とは異なり、多種多様な外来微生物に暴露する機会を有するユニークな臓器である。また、歯が粘膜を貫通し顎骨に植立しているため、歯周組織は上皮連続性が破綻した極めて特殊かつ脆弱なバリア部位であり、歯周病は人類史上最も罹患者数の多い感染症として知られている。歯周炎に伴い口腔細菌は血流に侵入し、感染性心内膜炎や動脈硬化、関節リウマチ、糖尿病など様々な全身疾患に悪影響を及ぼすと考えられているが、口腔細菌に対する免疫応答や生体防御機構に関しては不明な点が多い。
我々は、マウス歯周炎モデルを用いた解析から、歯周炎と同じく代表的な炎症性骨疾患である関節リウマチにおいて最強の悪玉と考えられてきた免疫細胞の亜集団が、口腔細菌依存的に歯周組織に集積し、感染制御に重要な役割を果たすことを明らかにした。具体的には、歯周炎組織において歯根膜細胞が産生するIL-6依存的に、本来は炎症抑制能を有するFoxp3陽性T細胞が、骨破壊誘導能の高い特殊なTh17細胞(exFoxp3Th17細胞)へと分化転換することを見出した。exFoxp3Th17細胞及びTh17細胞は、IL-17産生を介して口腔粘膜において抗菌ペプチドや好中球遊走因子の発現を誘導し、口腔細菌を量・質的に制御すると同時に、骨芽細胞や歯根膜細胞上に膜型RANKLの発現を誘導し、破骨細胞による歯槽骨吸収を促進した。興味深いことに、歯周炎を持続させたマウスでは口腔細菌による菌血症が生じたが、炎症性骨破壊に伴い感染歯を脱落させたマウスでは、遠隔臓器の感染及び口腔粘膜の炎症が終息した。以上の結果から、歯周炎組織に集積する骨破壊性T細胞(exFoxp3Th17細胞及びTh17細胞)は、粘膜免疫系を介した直接的な細菌制御と、骨免疫系を介した感染源(歯)の排除という二つの経路を介し、感染及び炎症を終息へと導く「諸刃の剣」であることが明らかとなり、炎症性骨破壊は単なる炎症の副次的効果ではなく、口腔細菌感染に対する生体防御機構としての役割を持つ可能性が示唆された(図)。
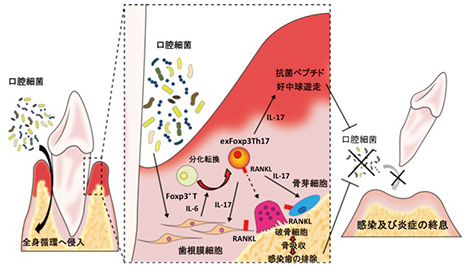
(図) “骨を壊して体を守る” 口腔粘膜のユニークな感染防御機構
歯は哺乳類にとって食事や戦闘に必須の臓器であるため、「感染源となった歯牙を脱落させ細菌から体を守るため、免疫の活性化は骨破壊を誘導するよう進化した」という概念は、一見合理性を欠くように思える。しかし上述のように、口腔粘膜を貫通し植立している歯の周囲は、多くの動物において感染に脆弱なバリア部位であること、哺乳類以外の脊椎動物は基本的に多生歯性(歯が生涯に何度も生え変わる)であり、古生代の爬虫類の化石からも歯周感染に伴う骨破壊及び歯の脱落の証拠が報告されていること(Reisz et al. Naturwissenschaften 98,551-555, 2011)を鑑みれば、炎症性骨破壊は歯が代替可能であった生物から保存されてきた、原始的な生体防御システムなのかもしれない。
著者コメント
歯周炎が進むと歯を支えている骨が破骨細胞により吸収され、最終的に歯は抜けてしまいます。これは患者さんや我々歯科医にとって最悪の事態なわけですが、患歯が脱落した後は粘膜の治癒に伴い、感染及び炎症が終息してくれるのも事実です。一方で、破骨細胞の機能不全である大理石骨病の患者が歯周炎に罹患した場合には、感染が持続し重篤な顎骨骨髄炎を発症すること、これは原因歯の抜去と抗生剤の投与により治癒することが報告されています。このような知見から、関節リウマチや癌骨転移の病態の鍵を握る「免疫が骨を壊す」という現象の起源は、生体で最も微生物の侵入を受けやすい歯周粘膜バリアに備わった、ユニークな生体防御機構なのではないかという、大胆な発想の転換に至りました。実験データや臨床的知見に基づきつつも、どこかdogmaticになりがちな私の仮説を「面白い」と言って下さり、scientificに昇華して下さった高柳広教授のご指導と、小松紀子先生をはじめとした共同研究者の先生方の温かいご協力に、この場をお借りして心より感謝申し上げます。本研究で得られた知見が、歯周炎や関節リウマチをはじめとした炎症性骨疾患の病態理解に、少しでも貢献できれば幸いです。(東京大学大学院医学系研究科 免疫学・塚崎 雅之)






