
[1] Gorlin 症候群患者で生じるヘッジホッグ関連遺伝子の多重変異が患者表現型に与える影響
[2] Gorlin 症候群由来iPS細胞はヘッジホッグを介した骨形成誘導に高い感受性をもつ
[2] Gorlin syndrome-derived induced pluripotent stem cells are hypersensitive to hedgehog-mediated osteogenic induction
| 著者: | [1] Onodera S et al [2] Hasegawa D et als |
|---|---|
| 雑誌: | [1] PLOS ONE 2017 vol: 12(9) pp: e0184702 [2] PLOS ONE 2017 vol: 12 (10) pp: e0186879 |
- 疾患iPS細胞
- 骨芽細胞
- 遺伝子変異解析

論文サマリー
Golrin症候群(基底細胞母斑症候群)は多発性の基底細胞癌(BCC)、石灰化歯原性嚢胞(OKC)および異所性の石灰化、骨形態異常を特徴とし、Hh受容体遺伝子PTCH1に変異を持つ常染色体優性遺伝性疾患である。Hh受容体PTCH1はHhが結合していない状態ではHh情報伝達経路を抑制する。Hhが結合するとその抑制機能が無くなり、Hh情報伝達が進行する。Gorlin症候群ではPTCH1変異のためPTCH1が本来もつHh経路抑制機能を喪失し、逆に恒常的に活性化することで病態が生ずると考えられている。本症候群は多臓器にわたり多彩な病態を持つにもかかわらず、遺伝子変異領域と症状には特別の関係が認められない。そこで、我々は本疾患遺伝子変異がPTCH1以外のHh情報経路にも重複して存在するか否か、次世代シークエンス技術を用いて遺伝子解析を行った。同時にヘッジホッグ情報経路恒常的活性化がもたらすGorlin症候群骨病変メカニズムの解明のために患者由来iPS細胞の樹立を行った。
KimonisのGorlin症候群診断基準により診断が確定し、インフォームドコンセントを得た4名の患者より採取したゲノムDNAを次世代シークエンス解析した。次世代シークエンス解析ではシークエンスを読んだ回数に相当するcoverageが多いほどシークエンスデータが確かと考えられるので、coverageが30以上あった変異を探索した。その結果4症例すべてでPTCH1遺伝子の変異を確認し、その内3症例は今まで報告のない新規変異であった。また、患者の線維芽細胞は正常人線維芽細胞に比べHh経路のターゲットであるGLI1遺伝子発現が上昇していることを確認したが、発現の程度は異なっていた。これまで、Hh遺伝子変異部位と症状には関連が無いといわれており、PTCH1以外のHh情報伝達経路の関連する遺伝子異常が重複して存在する可能性を疑い、Hh関連84遺伝子のデータを解析した。このとき遺伝子変異が機能的異常に関連するか否かを判定するMutationTasterおよびPolyphen2解析を行い タンパク質機能異常が強く疑われる遺伝子変異のみに着目した。すると面白いことにcase1にはPTCH1と遺伝子が54%相同であるPTCH2にも変異が重複して存在し、case3,4にはPTCH1,2とは異なるHh受容体であるBOCにも変異が存在することを確認した。Case2ではWnt9bに変異が存在した。Gorlin症候群ではPTCH2変異単独の報告もある。しかし、PTCH1変異が存在した場合その他のHh受容体変異は十分調べられていない可能性が高い。多彩なGorlin症候群疾患病態の背景には複数のHh受容体遺伝子変異やHh関連遺伝子変異が重複して存在し、結果としてHh経路の活性化の違いを生み異なる表現型を誘導する可能性もあると結論づけた。
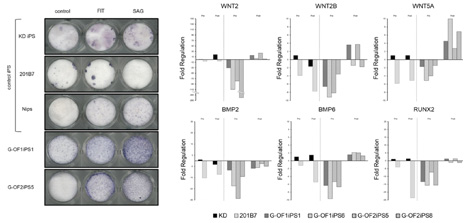
これら4症例の骨病変とHh関連遺伝子異常の関係を明らかにするため、iPS細胞を用いた検討を行った。患者由来iPS細胞はHh経路の活性化剤であるSAGに対し高い反応性を有していた。この細胞を用いて骨芽細胞分化を行うと、コントロールiPS細胞に比べALP活性が高く、骨芽細胞マーカーであるRUNX2発現が高かった。さらにiPS細胞においてはWNT、BMP群の遺伝子発現が低く、骨芽細胞誘導を行うとWNT、BMP群の遺伝子発現が優位に高くなることから、Golin症候群ではHh経路に加えWNT、BMP群も協調的に亢進させることで骨芽細胞誘導に過剰に反応し石灰化が亢進し骨組織病態を生じさせる可能性が考えられた。
著者コメント
歯科領域で多くみつかる疾患ということで注目しこの症候群についての検討を始めましたが、ゲノムの探索およびHh経路については今まで検討を行ったことがなく、一からのスタートとなりました。身近にいらっしゃる専門家の方々に教えていただきながら、なんとか論文出版にまでこぎつけました。本研究にあたり、ご指導いただきました多くの先生方にこの場を借りて深く感謝申し上げます。(東京歯科大学生化学講座・小野寺 晶子)






