
プロテインキナーゼN3はWnt5a-Ror2シグナルに応答して破骨細胞による骨吸収を促進する
| 著者: | Uehara S, Udagawa N, Mukai H, Ishihara A, Maeda K, Yamashita T, Murakami K, Nishita M, Nakamura T, Kato S, Minami Y, Takahashi N, Kobayashi Y |
|---|---|
| 雑誌: | Sci Signal. 2017 Aug 29;10(494). |
- 破骨細胞
- Wnt
- Pkn3

責任著者の小林教授(左)と筆者
論文サマリー
破骨細胞が骨吸収を行う時、細胞内のアクチン骨格が組み替えられ、リング状の構造(アクチンリング)が形成される。アクチンリング形成に関わるシグナル分子は、これまでに多数報告されている。その中には、低分子量Gタンパク質であるRhoも含まれるが、その役割には、不明な点が多い。
我々は、以前にWnt5aが破骨細胞前駆細胞のRor2受容体を介して破骨細胞分化を促進することを明らかにした。Ror2受容体は成熟破骨細胞にも発現しているので、骨吸収機能調節にも関与するのではないかと考え、Ror2 floxマウスとカテプシンK Creマウスを掛け合わせて破骨細胞特異的Ror2欠損(Ror2 cKO)マウスを作製した。このマウスは、骨吸収の低下による高骨量を呈した。Ror2 cKO破骨細胞は、アクチンリングを形成できず、骨吸収活性が低いことをin vitroの実験で確認した。
破骨細胞を、Wnt5aで刺激すると、RhoとRacの活性化が認められた。Ror2 cKO破骨細胞に恒常的活性型のRhoを発現させると骨吸収活性が回復したことから、Wnt5a-Ror2シグナルは、Rhoの活性化を介して骨吸収を促進すると考えた。
Rhoの下流で活性化されるRhoエフェクターは、13種類知られている。これらのうち、プロテインキナーゼN3 (Pkn3) の発現が、破骨細胞分化に伴い上昇することを、我々は見出した。Pkn3が生体内で破骨細胞機能に重要な役割を果たすか明らかにするため、Pkn3ノックアウト(KO)マウスの骨を解析し、骨吸収の低下による高骨量を呈することを明らかにした。
Pkn3と同じファミリーに属するPkn2は、SrcファミリーのキナーゼであるFynと結合することが報告されていた。また、Srcファミリーに属するc-Srcは破骨細胞のアクチンリング形成と骨吸収活性に重要である。そこで、Pkn3がc-Srcと結合し、骨吸収活性を促進するのではないかと仮説を立てた。免疫沈降法を用いた検討により、Pkn3は、Ror2シグナル依存的にc-Srcと結合することを見出した。さらに、Ror2 cKO及びPkn3 KO破骨細胞は、野生型破骨細胞と比べて、c-Srcの活性が低いことも明らかになった。
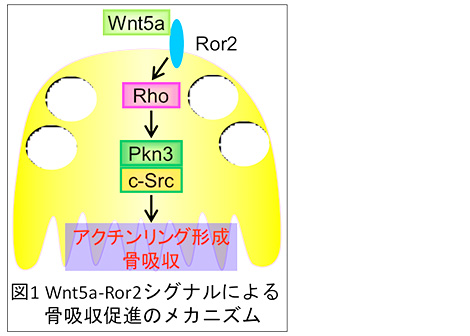
すなわち、Wnt5a-Ror2シグナルは、破骨細胞のRho-Pkn3経路を介してc-Srcの活性を亢進することで骨吸収を促進している、と結論した(図1)。
著者コメント
破骨細胞のRho、Rac活性の定量、shRNAをアデノウイルスで発現、マイクロCTで腰椎の骨量を定量と、研究室で実験系が確立していないことに体当たりでぶつかり試行錯誤の末どうにかここまでたどり着くことが出来ました。
データが全体的に地味だからグラフに色を付けた方が良いのでは、という小林先生の助言により、だいぶカラフルなFigになりました。あの色がまとめの図の色とリンクしていることに気づいてくれた人はいるでしょうか。
様々な紆余曲折を経た結果、非常に時間がかかりましたが、その間、温かい目で見守ってくださった宇田川先生、高橋先生、小林先生をはじめ、共著者の先生方、研究室と総合歯科医学研究所の皆様に感謝しています。(松本歯科大学 総合歯科医学研究所 硬組織機能解析学・上原 俊介)






