
NF-κB シグナルは軟骨細胞を両面的に制御する
| 著者: | Kobayashi H, Chang SH, Mori D, Itoh S, Hirata M, Hosaka Y, Taniguchi Y, Okada K, Mori Y, Yano F, Chung UI, Akiyama H, Kawaguchi H, Tanaka S, Saito T. |
|---|---|
| 雑誌: | Nat Commun. 2016 Nov 10;7:13336. |
- NF-κBシグナル
- 軟骨細胞

論文サマリー
我々は以前NF-κBシグナルが軟骨基質分解酵素であるADAMTS-5、転写因子 HIF-2αを誘導して変形性関節症を促進することを報告した。多様な生命現象を制御することが知られているNF-κBシグナルの軟骨における作用を解明するため、その主要な転写因子Rela/p65 に焦点をあてて解析を行った。
まず、軟骨内骨化においてNF-κBシグナルの成長板での解析を行った。軟骨特異的なCreマウスとRela-floxマウスをかけ合わせ、ホモノックアウトマウスを作成したところ、軽度の成長障害がみられた。その原因について解析したところ、骨端線増殖層における軟骨細胞のアポトーシスが亢進しており、軟骨細胞数が減少していた。一方、Relaをヘテロでノックアウトしたところ正常に成長した。
次に関節軟骨での解析を行った。成長後にRelaを軟骨特異的にホモノックアウトし、変形性関節症モデルや加齢による関節軟骨の変性を観察したところ、いずれの系においてもRelaを完全にノックアウトしたマウスは、HIF-2αやADAMTS-5の発現が抑えられていたにも関わらず、アポトーシスが亢進し変形性関節症が進行していた(図1)。
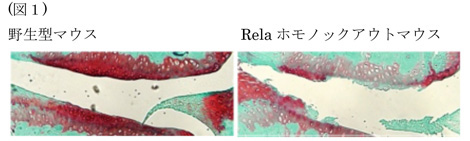
一方、Relaをヘテロでノックアウトしたマウスでは、逆に変形性関節症が抑えられ、HIF-2αやADAMTS-5の発現が減少していた(図2)。
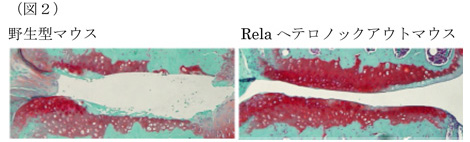
マイクロアレイによる網羅的解析の結果、Relaにより誘導される軟骨細胞の抗アポトーシス作用をもつ分子として、Traf2やcIAP1/2、p85αがあることが分かった。このうち、p85αは、PI3K のサブユニットであり、PI3K はAktの活性化を介してNF-κBシグナルを活性化することが知られていたが、これとは逆にNF-κBシグナルがPI3Kの主要サブユニットを直接的に転写誘導することを証明した。
最後に、Relaによって誘導される抗アポトーシス分子、HIF-2αやADAMTS-5は、RelaおよびNF-κBシグナル活性の量的な制御を受けており、NF- κBシグナルの活性が抑えられた状態ではRelaは抗アポトーシス分子を誘導することで軟骨細胞を保護しているが、NF-κBシグナルの活性が亢進した状態ではRelaは HIF-2αやADAMTS-5などの変性関連因子を誘導して関節軟骨を変性することが証明された。
以上のことから、NF-κBシグナルは、アポトーシスと変性関連因子の両面的な作用を有する分子を誘導することで軟骨細胞を両面的に制御していると考えられた。
著者コメント
私は東大整形外科入局後8年目で大学院に入り、軟骨細胞の基礎研究を始めました。研究開始当初は、カンファレンスで喋っている言語が全くわかりませんでしたが、研究室の諸先輩方のご指導のおかげで研究を遂行することができました。大学院4年間の間で、挫折を味わうことが多々ありましたが、研究室の同僚に支えられ、また、失敗に鈍感になりつつ、一方で新たな発見の喜びを時に感じながら基礎研究の魅力に取りつかれていました。現在は、臨床中心の生活を送っていますが、基礎研究で培ったマインドを元に未解決な問題に取り組んでいきたいと思います。(東京大学医学部附属病院整形外科 脊椎外科・小林 寛)






