
小胞体ストレストランスデューサーBBF2H7の小胞体内腔ドメインによる軟骨細胞増殖制御
| 著者: | Saito A, Kanemoto S, Zhang Y, Asada R, Hino K, Imaizumi K. |
|---|---|
| 雑誌: | Molecular Cell, 2014 Jan 9;53(1):127-139. |
- 軟骨細胞
- 細胞増殖
- 小胞体ストレストランスデューサー

論文サマリー
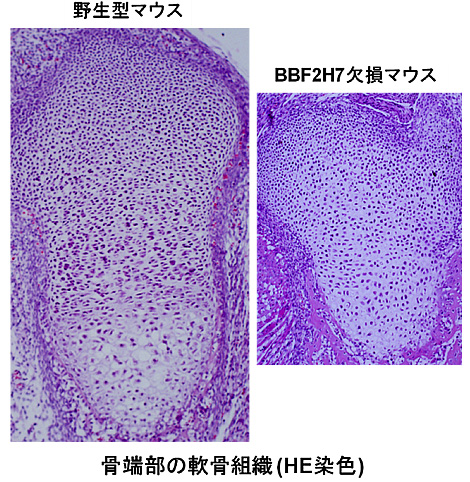
小胞体ストレストランスデューサーBBF2H7は小胞体膜上に局在する一回膜貫通型タンパク質で、軟骨細胞で強く発現している。このタンパク質は小胞体ストレスに応答して膜内切断を受け、DNA結合領域にあたるbasic leucine zipper領域を含むN末端断片が核内に移行し、転写因子として機能する。軟骨細胞におけるBBF2H7の転写ターゲットの一つは分泌タンパク質の小胞体-ゴルジ間輸送に必須のSec23aであり、BBF2H7欠損マウスはSec23aの減少によって軟骨基質タンパク質の分泌障害を伴う軟骨形成不全を示す。それに対してC末端断片の細胞内局在やその役割についてはわかっていなかった。我々はBBF2H7欠損マウスにおいて、すでに述べたような軟骨基質タンパク質の分泌障害に加え、軟骨細胞数が減少していることを見出した。初代培養軟骨細胞を採取して細胞増殖能を調べると、BBF2H7欠損細胞でBrdUの取り込みの減少、細胞周期関連遺伝子の発現減少、G1期からS期への進行抑制等が見られ、細胞増殖速度が低下していた。細胞増殖能が低下しているBBF2H7欠損細胞に転写因子として機能するN末端断片を発現させても細胞増殖速度は回復しなかったが、小胞体内腔側のC末端断片を発現させると野生型と同程度まで回復した。このことから、BBF2H7のC末端断片は細胞増殖を促進する機能をもつことがわかった。C末端断片の細胞内局在を調べると、切断後、小胞体から速やかに細胞膜近傍へ移動して細胞外へと分泌された。分泌されたC末端断片はヘッジホッグリガンドのIndian Hedgehogとその受容体であるPatched-1に結合してリガンド-レセプターコンプレックスの形成を促進することでヘッジホッグシグナルを活性化し、周辺細胞の増殖を促進させる機能をもつことがわかった。本研究によって、小胞体ストレス応答シグナルを介した細胞間コミュニケーションにおいて小胞体ストレストランスデューサー自身がシグナル伝達分子として機能するという新しいメカニズムが明らかになった。BBF2H7が強く発現している骨端軟骨組織の形成および伸長には、軟骨基質タンパク質の分泌促進による細胞外マトリックス領域の形成と、軟骨細胞の急速な増殖が極めて重要となる。BBF2H7は転写因子として機能するN末端断片が分泌経路の活性化を担うと同時に、細胞外に分泌されたC末端断片がヘッジホッグシグナルの活性化を介して急激な軟骨細胞の増殖を促している。BBF2H7はこの二つのメカニズムを二方向性の機能で同時に制御していることから、骨端軟骨組織の形成に必要不可欠な分子であるといえる。
著者コメント
私は大学院修士課程で今泉和則先生の研究室に参加させて頂いて以来、小胞体から発信されるシグナルによる生体制御機構の解析、特に骨格系組織形成と小胞体ストレス応答シグナルの関連性について研究を行ってきました。何も知らず、何もできなかったところから、遺伝子欠損マウスの扱いと解析法を学び、組織切片の作成法と観察法を知り、骨・軟骨細胞を扱い、少しずつ前進しながら今回の研究成果に辿りつくことができました。これもひとえに骨・軟骨研究に携わる多くの先生方のご助力と、今泉和則先生のご指導、そしてラボメンバーのサポートのおかげであります。多くの方々の支えに心より感謝申し上げます。(広島大学・齋藤 敦)






