
進行性骨化性線維異形成症における変異ACVR1の新たな機能
| 著者: | Kyosuke Hino, Makoto Ikeya, Kazuhiko Horigome, Yoshihisa Matsumoto, Hayao Ebise, Megumi Nishio, Kazuya Sekiguchi, Mitsuaki Shibata, Sanae Nagata, Shuichi Matsuda, and Junya Toguchida |
|---|---|
| 雑誌: | Proc Natl Acad Sci U S A. 2015 Nov 30 |
- iPS細胞
- 進行性骨化性線維異形成症
- 骨形成蛋白(BMP)

論文サマリー
進行性骨化性線維異形成症 (fibrodysplasia ossificans progressiva、以下FOP)は、筋、腱、靭帯といった線維性結合組織内に骨化巣が出現する非常に稀な遺伝性疾患である。外傷、外科的侵襲、感染などの炎症を惹起するエピソードにより骨化が劇的に進行するフレアーアップと称される現象を特徴とする。原因遺伝子は、BMPのⅠ型受容体の1つであるACVR1 (別名ALK2)の経配偶子性点突然変異であることがすでにわかっており、変異ACVR1 (以下FOP-ACVR1)のリガンド非依存的な恒常活性化能や、リガンド依存的な過剰活性化能が疾患の原因と考えられてきた。しかし、これら従来の仮説では、フレアーアップで骨化が劇的に進行するメカニズムが説明できない。このような背景から、FOPの本質的な原因が上記以外にあると着想し、今回、FOP-ACVR1のみでBMPシグナルを伝達するリガンドの同定を試み、その異所性骨形成における詳細なメカニズムを解析した。
まずはFOP患者由来iPS細胞と、そのFOP-ACVR1を野生型に修復したFOP患者由来iPS細胞をそれぞれ異所性骨形成の起源細胞の一つと考えられている、間葉系間質細胞 (FOP-及びresFOP-iMSCs)へと誘導し、BMP応答配列を用いたLuciferaseアッセイ (BRE-Luc assay)にてFOP-iMSCsのみでBMPシグナルを伝達するリガンドを探索した。BMPが含まれるTGF-βスーパーファミリーのリガンド約30種類についてのスクリーニングの結果、本来はBMPシグナルを伝達しないはずのActivin-AがFOP-iMSCsのみでBMPシグナルを伝達することが明らかとなった。Activin-Aは炎症時に分泌されることがわかっており、フレアーアップ時の骨化に関与している可能性があると考えられた。
FOPの異所性骨は、まず異所性の軟骨が出現し、続いてこれら軟骨が骨組織へと置換される内軟骨性骨化の様式で形成される。そこで次にActivin-Aの軟骨分化への作用をin vitroで検討した。まずは簡易なアッセイ系である2次元の軟骨分化アッセイを用いて、軟骨分化に重要なTGF-β3やBMP-7の作用とActivin-Aの作用を比較検討した。その結果、TGF-β3ではFOP-iMSCsとresFOP-iMSCsではほぼ同様の分化能を示し、BMP-7ではややFOP-iMSCsで分化亢進が認められたのに対し、Activin-Aで刺激すると、resFOP-iMSCsと比較しFOP-iMSCsにおいて顕著な軟骨分化が認められた。さらに、より成熟した軟骨を作製することが可能な3次元の軟骨ペレットアッセイでもActivin-Aの作用を検討したところ、FOP-iMSCs由来の軟骨ペレット内の細胞は肥大軟骨細胞の像を呈しており、より成熟した軟骨へと分化していることがわかった。
最後にin vivoでのActivin-Aの作用を検討するため、免疫不全マウス (NOD/SCID)にDoxycycline刺激に応じてActivin-Aを産生するC3H10T1/2細胞と、FOP-iMSCsあるいはresFOP-iMSCsを共移植し、6週間観察した。その結果、FOP-iMSCsを移植し、かつDoxycyclineでActivin-Aを誘導した部位でのみ、顕著な異所性骨が認められた (図)。この結果より、Activin-Aがin vivoで異所性骨形成を促進することが示された。
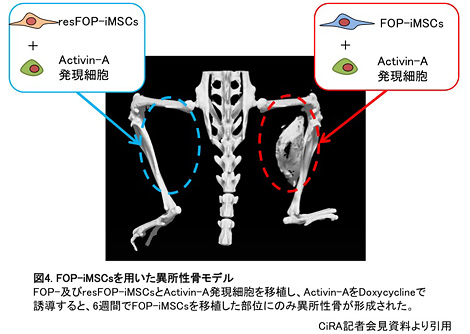
これらの結果から、FOP患者の異所性骨形成過程に予想外のリガンドであるActivin-Aが関与しているという新規のメカニズムが明らかになった。また、in vitro及びin vivoでFOP病態を反映した実験系が構築できたことから、今後はFOP患者由来iPS細胞を用いた創薬に進んでいきたいと考えている。
著者コメント
私は約2年半前に大日本住友製薬株式会社から京都大学iPS研究所 (CiRA)へと派遣され、FOP患者由来iPS細胞を用いた病態解明及び創薬を目標として研究をスタート致しました。戸口田淳也先生及び池谷真先生に熱心にご指導頂きました結果として、今回FOPの病態解明に関する論文を出すことができました。
実は今回の研究は、「iPS細胞の活用」がキーになったのです。FOP患者由来iPS細胞を用いた実験系は、FOP患者の生理的な条件に近いと考えられ、強制発現系と比較し、Activin-Aの作用を明確に検出できることがあとからわかりました。今後、まだ病態が解明されていない難病に関しても、iPS細胞を用いた解析で研究が進んでいくと期待しております。
私たちが独自に発見した、Activin-AがFOP-ACVR1のみでBMPシグナルを「間違って」伝達するという知見は、今まで説明がつかなかったFOP患者さんの病態をうまく説明できると考えております。今後はiPS細胞研究のアドバンテージを生かし、FOP患者由来細胞を用いた新規FOP治療剤のスクリーニングや、ヒット化合物の薬効評価に歩を進めていきたいと考えております。最後になりますが、このような研究の場と機会を与えて頂いた戸口田淳也先生及び池谷真先生に深く感謝申し上げます。(京都大学iPS細胞研究所・日野 恭介)






